ASCO 2020: Checkpoint-Inhibitoren bleiben im Fokus beim Urothelkarzinom
In der Zweitlinientherapie nach Versagen einer Cisplatin-basierten Vorbehandlung verlängern Checkpoint-Inhibitoren das Überleben im Vergleich zu herkömmlichen Zweitlinien-Chemotherapien und sind aktueller Therapiestandard in dieser Indikation. Es ist daher nur konsequent, dass Checkpoint-Inhibitoren in weiteren Therapieindikationen bei Urothelkarzinomen untersucht werden. An der diesjährigen Jahrestagung der American Society of Clinical Oncology (ASCO) wurden die Ergebnisse von zwei grossen prospektiven randomisierten Studien vorgestellt. Keimzelltumoren wurden dagegen nur in kleineren Serien retrospektiv untersucht. Dennoch sind die Ergebnisse einiger Poster interessant und unterstützen die derzeitigen Anstrengungen, die Therapie auch dieser Patientengruppe weiter zu verbessern.
Keypoints
-
Eine Erhaltungstherapie mit Avelumab verlängert das Überleben metastasierter Patienten mit Urothelkarzinomen und Ansprechen auf eine Platin-basierte Erstlinienherapie.
-
Die adjuvante Gabe von Atezolizumab zeigt keinen Vorteil im krankheitsfreien Überleben oder Gesamtüberleben nach kurativ intendierter Resektion bei Patienten mit Urothelkarzinomen der Harnblase, des Ureters oder des Nierenbeckens.
-
Eine prophylaktische Antikoagulation kann das Auftreten lebensbedrohlicher Thrombembolien bei Patienten mit metastasierten Keimzelltumoren reduzieren.
Urothelkarzinom – adjuvante Therapie
Die perioperative Therapie bei kurativintendierter radikaler Zystektomie stellt eine der wichtigsten Indikationen für eine Systemtherapie bei Patienten mit Urothelkarzinomen dar, da mit einer Reduktion der hohen Rezidivrate zusätzliche Patienten geheilt werden können. Im Gegensatz zur neoadjuvanten Therapie ist der Nutzen einer adjuvanten Platin-basierten Therapie jedoch umstritten. Daher werden die Ergebnisse der drei grossen randomisierten Studien mit Spannung erwartet, welche den Einsatz der Checkpoint-Inhibitoren Atezolizumab (Akronym: IMVigor10), Nivolumab (Akronym: CheckMate 274) und Pembrolizumab (Akronym: AMBASSADOR) untersuchen. Die Auswertung der Wahrscheinlichkeit des krankheitsfreien Überlebens (DFS) und die erste Zwischenauswertung der Gesamtüberlebenswahrscheinlichkeit (OS) der IMVigor10-Studie zur adjuvanten Therapie mit Atezolizumab liegen jetzt vor.
IMVigor10-Studie1
Eingeschlossen werden konnten Patienten mit fortgeschrittenen Urothelkarzinomen der Blase, des Ureters oder des Nierenbeckens mit oder ohne Lymphknotenbefall, unabhängig davon, ob sie eine neoadjuvante Chemotherapie erhalten hatten oder nicht. Patienten ohne neoadjuvante Chemotherapie mussten allerdings Kontraindikationen gegenüber einer Cisplatin-basierten Therapie vorweisen oder eine solche Therapie abgelehnt haben. Eingeschlossen werden konnten Patienten mit kurativintendierter kompletter Resektion und einem Performance Status der Eastern Cooperative Group (ECOG) von 0–2. Nur zu Beginn der Studie war eine hohe Expression von PD-L1 («programmed cell death ligand 1») als Einschlusskriterium gefordert.
Die Randomisierung war nach den wichtigsten Prognosefaktoren stratifiziert. Randomisiert wurden 809 Patienten: 406 Patienten im Studienarm mit adjuvanter intravenöser Gabe von Atezolizumab 1200mg Absolutdosis alle drei Wochen für insgesamt 16 Zyklen bzw. ein Jahr sowie 403 Patienten im Studienarm mit alleiniger Nachbeobachtung. Die Studie war somit nicht placebokontrolliert und nicht verblindet.
In beiden Studienarmen traten in Bezug auf das DFS mit 52% gleich viele Ereignisse auf. Das mediane DFS mit adjuvanter Gabe von Atezolizumab unterschied sich mit 19,4 Monaten nicht signifikant vom medianen DFS im Beobachtungsarmmit 16,6 Monaten bei einer Hazard-Ratio (HR) von 0,89 (p=0,2446).
Das primäre Studienziel von IMVigor10 wurde damit nicht erreicht. Auch die DFS-Rate nach 18 Monaten war mit 51% und 49% in den beiden Studienarmen statistisch nicht signifikant unterschiedlich.
Die Nachbeobachtungszeit in der IMVigor10-Studie ist noch kurz. In Bezug auf das OS traten daher nur in 29% bzw. 31% Ereignisse auf, und das mediane OS wurde in beiden Studienarmen nicht erreicht. Allerdings war auch die OS-Rate nach 18 Monaten mit 79% bzw. 73% in den beiden Studienarmen statistisch nicht signifikant unterschiedlich (Tab. 1).
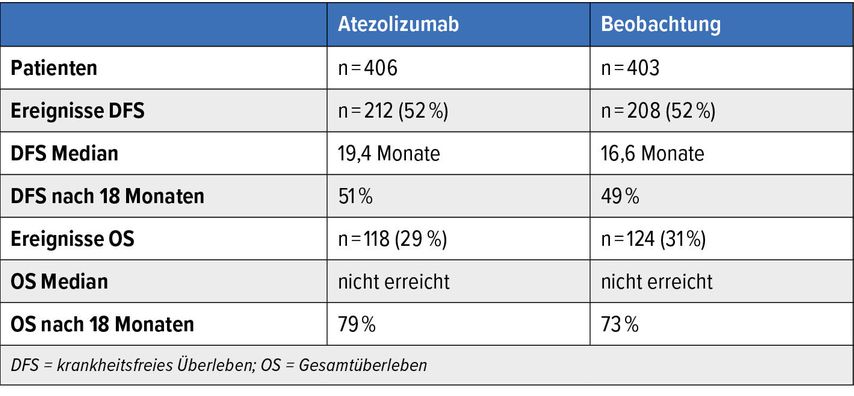
Tab. 1: Übersicht IMVigor10-Studie (nach Hussain MHA et al.)1
In keiner der prädefinierten Subgruppen konnte ein Vorteil im DFS nachgewiesen werden. Auch Patienten mit einer höheren PD-L1-Expression profitieren von der adjuvanten Therapie mit Atezolizumab in Bezug auf das DSF nicht. Atezolizumab wurde mit den aus vorgängigen Studien bekannten Nebenwirkungen gut vertragen. Immunvermittelte Nebenwirkungen Grad 3–4 traten bei unter 10% der Patienten auf und waren somit selten. Ein Patient im Studienarm mit Atezolizumab starb an ARDS.
Insgesamt enttäuscht der Einsatz von Atezolizumab in der adjuvanten Therapieindikation. Auch mit längerer Nachbeobachtung ist keine grundlegende Änderung dieser Einschätzung zu erwarten. Die Ergebnisse der Studie CheckMate 274 und der AMBASSADOR-Studien zum Einsatz von Nivolumab bzw. Pembrolizumab stehen aus.
Urothelkarzinom – Erstlinientherapie metastasierter Patienten
Eine Cisplatin-basierte Erstlinien-Chemotherapie ist unverändert Standard bei Patienten mit metastasierten Urothelkarzinomen: Circa 85% der Patienten sprechen an oder erreichen zumindest eine Krankheitsstabilisierung, ca. 15% sind trotz Cisplatin-haltiger Erstlinien-Chemotherapie progredient. Aber auch Patienten mit Ansprechen auf Erstlinien-Chemotherapie sind in der Regel innerhalb weniger Monate erneut progredient. Das mediane Überleben nach Cisplatin-basierter Erstlinien-Chemotherapie beträgt nur ca. ein Jahr. Allerdings ist ein Langzeitüberleben von mehreren Jahren bei ca. 10–15% der Patienten zu erwarten. Schlechtere Ergebnisse werden mit Carboplatin-basierter Therapie erzielt.
Studie JAVELIN Bladder 1002
In dieser Studie wurden insgesamt 700 Patienten mit nicht resezierbaren oder metastasierten Urothelkarzinomen in einer offenen, nicht verblindeten, prospektiven Studie nach 4–6 Zyklen Platin-basierter Chemotherapie(Cisplatin oder Carboplatin) randomisiert; jeweils 350 Patienten pro Studienarm. Patienten, die mit einer kompletten Remission (CR) oder einer partiellen Remission (PR) angesprochen hatten oder zumindest eine Stabilisierung ihrer Erkrankung (SD) aufwiesen, erhielten in der Studie entweder eine intravenöse Erhaltungstherapie mit Avelumab 10mg/kg alle 2 Wochen bis zum Progress oder bis zum Auftreten nicht akzeptabler Nebenwirkungen oder sie wurden mit alleiniger «best supportive care» betreut. Ein Cross-over zu Avelumab bei Progress war im Studienarm mit «best supportive care» nicht vorgesehen, und überhaupt erhielten nur ca. 50% der Patienten in dem Studienarm mit «best supportive care» einen Checkpoint-Inhibitor als Zweitlinientherapie.
Das mediane OS lag im Studienarm mit Avelumab-Erhaltungstherapie bei 21,4 Monaten gegenüber 14,3 Monaten im Studienarm mit «best supportive care». Somit entsprach das OS im Studienarm mit «best supportive care» demjenigen, welches nach verfügbarer Evidenz nach Platin-basierter Therapie zu erwarten gewesen wäre, das OS unter Erhaltungstherapie mit Avelumab war statistisch signifikant und klinisch relevant länger, mit einer HR von 0,69 (p<0,001). Der Vorteil im OS zugunsten der Erhaltungstherapie mit Avelumab betraf alle Subgruppen von Patienten. Auch die Ansprechrate und die Wahrscheinlichkeit des progressionsfreien Überlebens (PFS) waren unter Avelumab statistisch signifikant höher (Tab. 2).
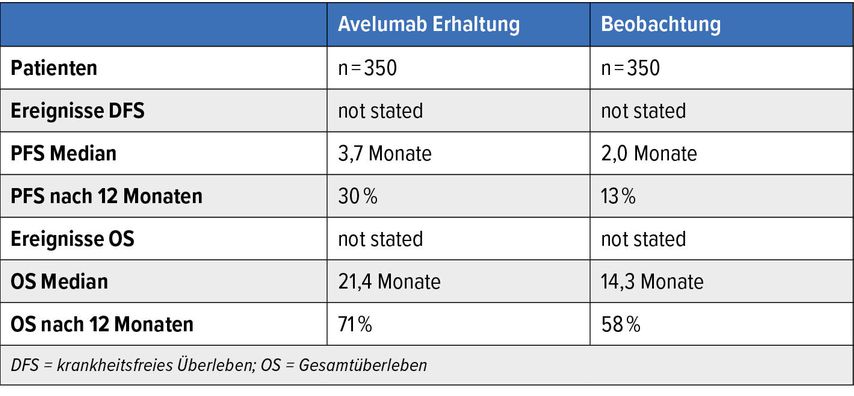
Tab. 2: Übersicht JAVELIN-100-Studie (nach Powles T et al.)2
Die Subgruppe von Patienten mit hoher Expression von PD-L1 schnitt in beiden Studienarmen noch besser ab: Das mediane OS wurde unter Avelumab nicht erreicht, unter «best supportive care» betrug es 17,1 Monate.
Die Verträglichkeit einer Erhaltungstherapie mit Avelumab war gut. Weniger als 10% der Patienten erlittenimmunvermittelte Nebenwirkungen Grad 3, Nebenwirkungen vom Grad 4 oder therapieassoziierte Todesfälle traten nicht auf.
Eine Erhaltungstherapie mit Avelumab stellt somit für die Mehrheit der Patienten mit metastasierten Urothelkazinomen und Ansprechen auf eine Platin-basierte Erstlinientherapie einen möglichen neuen Therapiestand dar. Allerdings bleiben viele Fragen offen.
Erstens ist eine Erhaltungstherapie mit Avelumab eine teure Übertherapie derjenigen 10–15% Patienten, die bereits nach alleiniger Cisplatin-haltiger Chemotherapie ein Langzeitüberleben erzielt hätten. Zweitens erhielt nur etwa die Hälfte der Patienten im Studienarm mit «best supportive care» als Zweitlinientherapie einen Checkpoint-Inhibitor, von dem sie hätten profitieren können. Drittens hatten Patienten mit Progress nach Erhaltungstherapie mit Avelumab in der zweiten Linie nur selten einen anderen Checkpoint-Inhibitor erhalten, und nur ca. 40% der Patienten hatten eine konventionelle Chemotherapie erhalten. Welche effektiven Therapieoptionen verbleiben noch bei Progress der mit Erhaltungstherapie behandelten Patienten? Der unstrittige Vorteil einer Erhaltungstherapie liegt in der Verlängerung des PFS und damit gegebenenfalls im Hinauszögern des Auftretens Tumor-bedingter Beschwerden um ca. 2–3 Monate. In Ländern wie der Schweiz, in denen eine Zweitlinientherapie mit einem Checkpoint-Inhibitor breit verfügbar ist, bleibt dennoch nach der aktuellen Datenlage unverändert die Therapiealternative, mit dem Einsatz eines Checkpoint-Inhibitors bis zur zweiten Linie zu warten.
Hodentumoren
Patienten mit metastasierten Hodentumoren werden in der überwiegenden Mehrzahl durch 3–4 Zyklen Cisplatin-basierte Chemotherapie geheilt. Dennoch werden unter dieser Therapie vermehrt zum Teil lebensbedrohliche venöse Thrombembolien beobachtet. Die genaue Ursache ist unklar. Risikofaktoren sind neben der Zahl Cisplatin-haltiger Zyklen ein grosser abdomineller Tumor von mehr als 5cm Durchmesser sowie möglicherweise ein erhöhter Khorana-Score, ein hoher Body-Mass-Index und zentralvenöse Katheter.3
Ein Poster einer internationalen Studiengruppe unter Schweizer Leitung hat Risikofaktoren untersucht und empfiehlt bei allen Patienten mit metastasierten Hodentumoren während Chemotherapie eine medikamentöse Thromboseprophylaxe.4 Die Daten werden aktuell von einem weiteren Poster unterstützt, welches den Einsatz von niedermolekularen Heparinen mit neuen oralen Antikoagulanzien bei ambulanten Krebspatienten vergleicht und weniger Blutungskomplikationen bei Einsatz neuer oraler Antikoagulanzien findet, bei gleicher Wirksamkeit wie unter Heparinen.5
Fazit
Die optimale Strategie des Einsatzes von Checkpoint-Inhibitoren bei Urothelkarzinomen ist unverändert offen. Neben dem gesicherten Einsatz in der zweiten Linie nach Versagen einer Platin-basierten Chemotherapie ist eine Erhaltungstherapie mit Avelumab bei Ansprechen auf eine Platin-basierte Erstlinienchemotherapie eine mögliche neue Alternative. Eine adjuvante Therapie mit Atezolizumab nach radikaler Zystektomie zeigt dagegen keinen statistisch nachweisbaren Nutzen.
Autoren:
Prof. Dr. med. Jörg Beyer
Medizinische Onkologie
Inselspital, Universität Bern
E-Mail: joerg.beyer@insel.ch
Prof. Dr. med. Anja Lorch
Klinik für Onkologie
UniversitätsSpital Zürich
E-Mail: anja.lorch@usz.ch
Literatur:
1 Hussain MHA et al.: IMvigor010: Primary analysis from a phase III randomized study of adjuvant atezolizumab (atezo) versus observation (obs) in high-risk muscle-invasive urothelial carcinoma (MIUC). J Clin Oncol 38: 2020 (suppl; abstr 5000) 2 Powles T et al.: Maintenance avelumab + best supportive care (BSC) versus BSC alone after platinum-based first-line (1L) chemotherapy in advanced urothelial carcinoma (UC): JAVELIN Bladder 100 phase III interim analysis. J Clin Oncol 38: 2020 (suppl; abstr LBA1) 3 Lyman GH et al.: Venous thromboembolism prophylaxis and treatment in patients with cancer: American Society of Clinical Oncology clinical practice guideline update. J Clin Oncol 2013, 31:2189-2204 4 Fankhauser CD et al.: Benefit of prophylactic anticoagulation before and during first-line chemotherapy on patients with metastatic germ cell tumors. J Clin Oncol 2020; 38 (suppl 6; abstr 402) 5 Shenouda M et al.: Efficacy and safety of direct oral anticoagulants (DOACs) and low molecular weight heparin (LMWH) for primary prevention of venous thromboembolism (VTE) in ambulatory cancer patients. J Clin Oncol 2020; 38 (suppl; abstr 12088)
Das könnte Sie auch interessieren:
Seltener Tumor, hohe Mortalität
Eine 88-jährige Frau präsentiert sich mit einer Hautveränderung im Gesicht: einer erbsengroßen, glasigen Papel. Diagnostiziert wird ein Hauttumor, der vor allem ab dem 60. Lebensjahr ...
HIV-Diagnostik: Die Unterstützung vonseiten der Dermatologie ist gefragt!
Etwa 40% der HIV-Erstdiagnosen in Österreich werden zu einem Zeitpunkt gestellt, zu welchem das Immunsystem der Patient:innen bereits stark beeinträchtigt ist.1 Solche späten Diagnosen ...
Vitiligo: mit Ausdauer und Kombinationstherapien zum Erfolg
Rasche Diagnosesicherung und Therapieeinleitung sind bei der Vitiligo essenziell, auch aufgrund der individuellen Belastungssituation vieler Patient:innen. Vier Therapieziele, die ...