Neue Therapieoptionen verbessern Prognose bei Mammakarzinom
Beim virtuellen Jahreskongress 2020 der American Association for Cancer Research (AACR) wurden unter anderem interessante neue Daten zur Therapie des HER2-negativen und des metastasierten tripelnegativen Mammakarzinoms präsentiert. Vorgestellt wurden
unter anderem die Studien I-SPY 2, EMBRACA und IMPRIME 1.
Keypoints
-
Die Kombination aus dem PD- L1-Antikörper Durvalumab und dem PARP-Inhibitor Olaparib mit Paclitaxel verbessert das Outcome gegenüber Paclitaxel- Monotherapie.
-
Der PARP-Inhibitor Talazoparib führte im Vergleich zur Chemotherapie zu keiner Verlängerung des Gesamtüberlebens.
-
Die Zugabe des Immun- aktivators Imprime PGG zu Pembrolizumab verlängerte PFS und OS.
I-SPY 2: HER2-negatives Hochrisiko-Mammakarzinom
Prof. Lajos Pusztai, Yale Cancer Center, New Haven (USA), präsentierte die Ergebnisse der Phase-II-Studie I-SPY-2, in der die Kombination aus dem PD-L1-Antikörper Durvalumab und dem PARP-Inhibitor Olaparib mit Paclitaxel bei Patientinnen mit HER 2-negativem Hochrisiko-Mammakarzinom Stadium II/III untersucht wurde. Primärer Endpunkt war die pathologische Komplettremission (pCR), definiert als ypT0/is und ypN0 (kein invasiver Tumor in der Brust oder Lymphknoten nachweisbar). Einschlusskriterien waren eine Tumorgröße >2,5cm, HER2-Negativität und ein Performancestatus <2. Hormonrezeptor(HR)-positive Patientinnen konnten eingeschlossen werden, wenn sie im MammaPrint-Test ein hohes Risiko aufwiesen.1
Durvalumab konnte in früheren Studien als neoadjuvante Therapie in Kombination mit nab-Paclitaxel und Doxorubicin/Cyclophosphamid die Rate an vollständigen Remissionen bei Patientinnen mit tripelnegativem Mammakarzinom (TNBC) steigern. Olaparib verlängerte als Zweit- oder Drittlinientherapie bei BRCA-mutiertem Brustkrebs (Hormonrezeptor-positiv und TNBC) das progressionsfreie Überleben (PFS) signifikant. Die Rationale für die Kombination der beiden Substanzen ist, dass die gestörten DNA-Reparaturmechanismen durch die PARP-Hemmung in den Krebszellen zu vermehrten Mutationen und Neoantigenen führen. Die DNA-Fragmente aktivieren den intrazellulären Pathway STING („stimulator of interferon genes“) und damit die körpereigene Immunabwehr. Die PARP-Hemmung kann aber auch direkt die PD-L1-Expression in Mammakarzinom-Zelllinien hochregulieren. Die Kombination wurde bereits erfolgreich auf ihre Sicherheit bei metastasiertem BRCA-mutiertem Brustkrebs getestet, wie Pusztai erläuterte.1
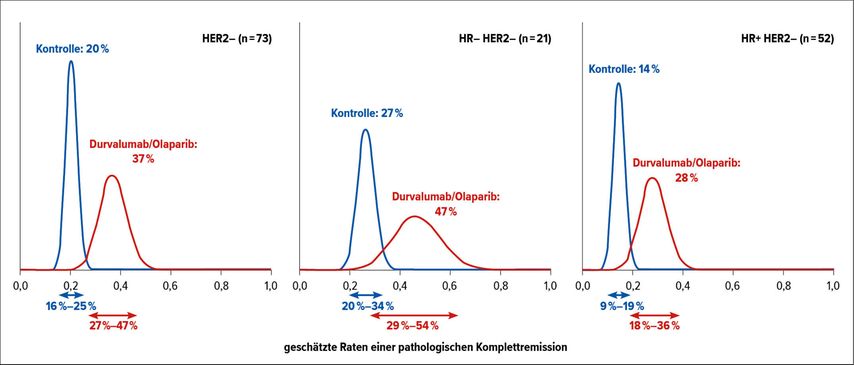
Für I-SPY 2 wurden 73 Patientinnen in den Durvalumab/Olaparib-Arm aufgenommen, davon waren 21 HR– und 52 HR+. Die Kontrollgruppe bestand aus 299 Patientinnen, die Paclitaxel erhielten. Die Durvalumab/Olaparib-Kombination erhöhte die pCR-Wahrscheinlichkeit gegenüber der Kontrollgruppe deutlich (Abb. 1): Für alle HER2- negativen Patientinnen lag sie bei 37% (vs. 20%), für HR–/HER2– bei 47% (vs. 27%) und für HR+/HER2– bei 28% (vs. 14%).1
EMBRACA: finale OS-Daten
Prof. Jennifer Litton, MD Anderson Cancer Center, Houston/Texas, stellte die finale Analyse zum Gesamtüberleben (OS) von EMBRACA vor, der derzeit größten Studie mit Talazoparib bei Patientinnen mit fortgeschrittenem Brustkrebs und BRCA1/2-Mutationen.2
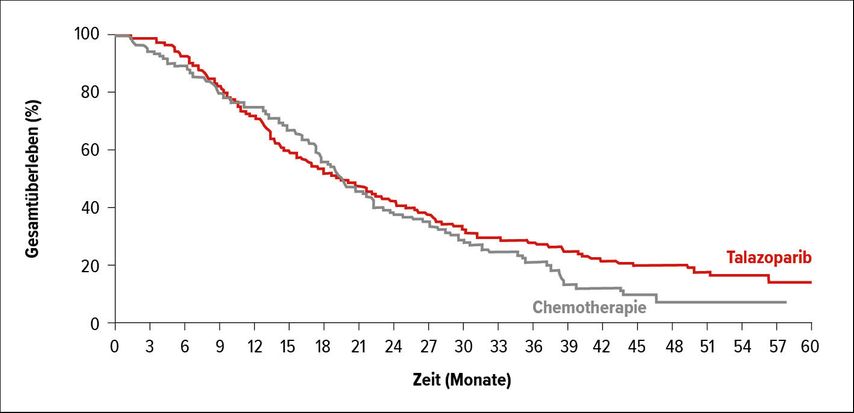
Insgesamt nahmen 431 Patientinnen mit BRCA-mutiertem HER2-negativem lokal fortgeschrittenem und/oder metastasiertem Brustkrebs teil. Sie erhielten entweder den PARP-Inhibitor Talazoparib oder Chemotherapie nach der Wahl des behandelnden Arztes (Capecitabin, Eribulin, Gemcitabin oder Vinorelbin). Primärer Endpunkt war das PFS. Das OS war ein Haupt-Sekundärendpunkt. Während Talazoparib das PFS signifikant verlängern konnte (8,6 v. 5,6 Monate; p<0,0001),3 war beim OS kein statistisch signifikanter Unterschied feststellbar (Abb. 2). Allerdings fielen die „patient-reported outcomes“ (PRO) – wie schon zuvor – zugunsten von Talazoparib aus.2,3 Im Vergleich zu den Ausgangswerten verbesserte sich die Lebensqualität, erfasst mit dem GHS/QoL-Fragebogen, im Talazoparib-Arm um 2,1 Punkte, während sie im Chemotherapie-Arm um 5,7 Punkte abnahm (p=0,001). Für Patientinnen mit fortgeschrittenem BRCA-mutiertem HER2- negativem Mammakarzinom ist Talazoparib daher eine geeignete Therapieoption.2
IMPRIME 1
Dr. Steven O’Day, John Wayne Cancer Institute, Santa Monica, USA, zeigte die Resultate der Phase-II-Studie IMPRIME, in der Pembrolizumab mit einem neuartigen Immunaktivator (Imprime PGG) bei metastasiertem TNBC (mTNBC) untersucht wurde.4 Imprime PGG ist ein Betaglucan, das aus der Zellwand von Saccharomyces isoliert wurde. Es bildet Immunkomplexe, indem es endogene Anti-Beta-Glucan-Antikörper (ABA) bindet. Der Immunkomplex ist der aktive Wirkstoff, der durch die Bindung an Dectin-1-Rezeptoren und Korezeptoren eine Antitumorwirkung entfaltet. Es kommt zu einer Veränderung der Mikroumgebung des Tumors, zur Aktivierung Antigen-präsentierender Zellen sowie zu einer verstärkten tumorspezifischen T-Zell-Aktivität und -Infiltration.4 In die Studie IMPRIME wurden 44 nicht mit einer Immuncheckpoint-Therapie vorbehandelte mTNBC-Patientinnen eingeschlossen, die mindestens eine vorangegangene Chemotherapie erhalten hatten. Zudem wurde der ABA-Spiegel bestimmt, der >20 Mikrogramm/ml liegen musste. Primärer Endpunkt war die Gesamtansprechrate (ORR), sekundäre Endpunkte waren Sicherheit, OS, PFS und Krankheitskontrollrate (DCR). Tabelle 1 zeigt die Ergebnisse der Studie.
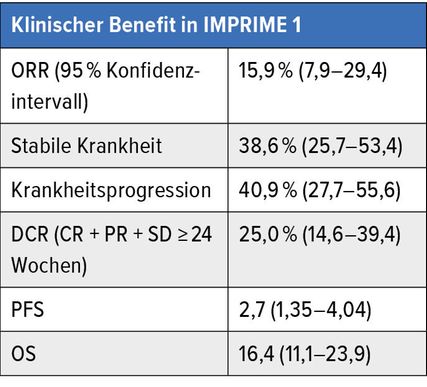
Tab. 1: Klinischer Benefit in IMPRIME 1 (n=44)
Im Blut konnte bereits drei Wochen nach Therapiebeginn eine Aktivierung des Immunsystems nachgewiesen werden, zum Beispiel vermehrt CD86 auf zirkulierenden Monozyten und eine CD8-T-Zell-Aktivierung (PD1+/Ki67+/HLA-DR+). Dies ging mit verlängertem PFS und OS einher. Tumorbiopsien zeigten eine robuste Infiltration des Gewebes durch aktivierte Immunzellen. Dabei wurde die Therapie gut vertragen. Dies rechtfertige größere kontrollierte Studien, schloss O’Day.
Bericht:
Dr. Corina Ringsell
Quelle:
AACR Virtual Annual Meeting I, 27.–28. April 2020
Literatur:
1 Pusztai L et al.: Evaluation of durvalumab in combination with olaparib and paclitaxel in high-risk HER2 negative stage II/III breast cancer: Results from the I-SPY 2 TRIAL. AACR Virtual Meeting 2020, Abstr. CT011 2 Litton JK et al.: Talazoparib (TALA) in germline BRCA1/2 (gBRCA1/2)-mutated human epidermal growth factor receptor 2 negative (HER2-) advanced breast cancer (ABC): final overall survival (OS) results from randomized Phase 3 EMBRACA trial. AACR Virtual Meeting 2020, Abstr. CT071 3 Litton JK et al.: Talazoparib in patients with advanced breast cancer and a germline BRCA mutation. N Engl J Med 2018; 379: 753-63 4 O’Day SJ et al.: IMPRIME 1 (NCT02981303): a novel phase 2 study in second-line +, metastatic triple negative breast cancer patients shows promising clinical benefit for the combination of the immune checkpoint inhibitor, pembrolizumab (pembro), with the novel innate immune activator, Imprime PGG. AACR Virtual Meeting 2020, Abstr. CT073
Das könnte Sie auch interessieren:
HIV-Diagnostik: Die Unterstützung vonseiten der Dermatologie ist gefragt!
Etwa 40% der HIV-Erstdiagnosen in Österreich werden zu einem Zeitpunkt gestellt, zu welchem das Immunsystem der Patient:innen bereits stark beeinträchtigt ist.1 Solche späten Diagnosen ...
Vitiligo: mit Ausdauer und Kombinationstherapien zum Erfolg
Rasche Diagnosesicherung und Therapieeinleitung sind bei der Vitiligo essenziell, auch aufgrund der individuellen Belastungssituation vieler Patient:innen. Vier Therapieziele, die ...
Periphere Nervenscheidentumoren
Periphere Nervenscheidentumoren sind eine seltene, aber dennoch bedeutende Tumorentität, die das periphere Nervensystem betrifft. Sie können eine Vielzahl an Symptomen verursachen und ...