Krebstherapie: was tun, um kardiologische Nebenwirkungen zu minimieren?
Bericht:
Reno Barth
Im Rahmen ihres diesjährigen Kongresses stellte die ESC erstmals eine Leitlinie zum Thema Kardioonkologie vor. Themenschwerpunkt der Guideline ist das Management kardialer Nebenwirkungen onkologischer Therapien. Dargestellt werden Behandlungsalgorithmen für jede Klasse onkologischer Medikamente und das Monitoring von Patienten, das bei manchen lebenslang erfolgen sollte.1
Onkologische Therapien haben häufig kardiologische Nebenwirkungen und können zu irreparablen Schädigungen des Herzens führen. Dies gilt für jeweils bestimmte Chemotherapien, gezielte Therapien und Immuntherapien, ebenso wie für die Strahlentherapie. „Die zentralen Ziele der ersten ESC-Leitlinie zum Thema Kardioonkologie, die von der Europäischen Kardiologengesellschaft gemeinsam mit den Fachgesellschaften EHA (European Hematology Association), ESTRO (European Society for Therapeutic Radiology and Oncology) und IC-OS (International Cardio-Oncology Society) herausgegeben wird, bestehen darin, die dynamische Natur der kardiologischen Toxizitäten onkologischer Therapien zu vermitteln und auf die Notwendigkeit einer individualisierten Behandlung der betroffenen Patienten hinzuweisen“, so die Vorsitzende der „Guideline-Taskforce“ Prof. Teresa Lopez-Fernandez vom La Paz Universitätsspital in Madrid. „Diese Leitlinie richtet sich an Gesundheitsberufe, die Krebspatienten und -überlebende betreuen. Sie fasst spezifische Empfehlungen zum Management vor, während und nach onkologischen Therapien, die das Potenzial haben, Herz und Gefäße zu schädigen, zusammen“, wie einer der Leitlinienautoren, Dr. Alexander Lyon vom Royal Brompton Hospital in London erklärt. Diese Betreuung kann langfristig erforderlich sein. Denn aufgrund der lebensverlängernden Wirkungen moderner onkologischer Therapien gibt es viele Langzeitüberlebende, die aufgrund der erfolgreichen Behandlung ihres Tumors lange Zeit mit einer kardialen Schädigung leben. Bei Langzeitüberlebenden nach verschiedenen soliden Tumoren sowie Lymphomen ist das Risiko im Vergleich zu gesunden Kontrollen auf rund das Doppelte erhöht. Daher besteht die erste Herausforderung einmal darin, zu wissen, welche onkologischen Therapien mit kardialen Risiken assoziiert sind.
„Cancer therapy-related cardiac dysfunction“ (CTRCD)
Mögliche Schädigungen des kardiovaskulären Systems können sowohl die Gefäße als auch das Myokard betreffen. Konsequenzen von der Klappenerkrankung über die Myokarditis bis zur arteriellen oder pulmonalen Hypertonie sind möglich. Das individuelle Risiko richtet sich nach dem Alter, der onkologischen Krankengeschichte, kardiovaskulären Risikofaktoren, bestehenden kardiovaskulären Erkrankungen sowie kardiotoxischen Therapien in der Anamnese – und natürlich nach Art und Dauer der kardiotoxischen onkologischen Therapie. Die neue Leitlinie soll nun, so Lopez-Fernandez, helfen, durch Therapieoptimierung das Risiko von Therapieunterbrechungen zu minimieren, sowie kardioprotektive Maßnahmen und das Follow-up der Patienten verbessern. Um diese Ziele zu erreichen, wurde der aktuelle Evidenzstand in 272 neuen Empfehlungen zusammengefasst. Dazu wurde zunächst der neue Begriff der „cancer therapy-related cardiac dysfunction“ (CTRCD) eingeführt, der das breite Spektrum der kardialen Folgeerscheinungen onkologischer Therapien abdecken soll. CTRCD kann symptomatisch oder asymptomatisch und unterschiedlich ausgeprägt sein. Grundsätzlich wird empfohlen, vor Beginn einer onkologischen Therapie eine gründliche kardiologische Abklärung vorzunehmen, um Risikopatienten zu identifizieren. Diese sollten anschließend an einen Kardiologen zur weiteren Evaluation und Optimierung der Risikofaktoren überwiesen werden. Um keine Zeit zu verlieren, sollte diese Abklärung unmittelbar nach der Krebsdiagnose erfolgen.
Einteilung in Risikogruppen
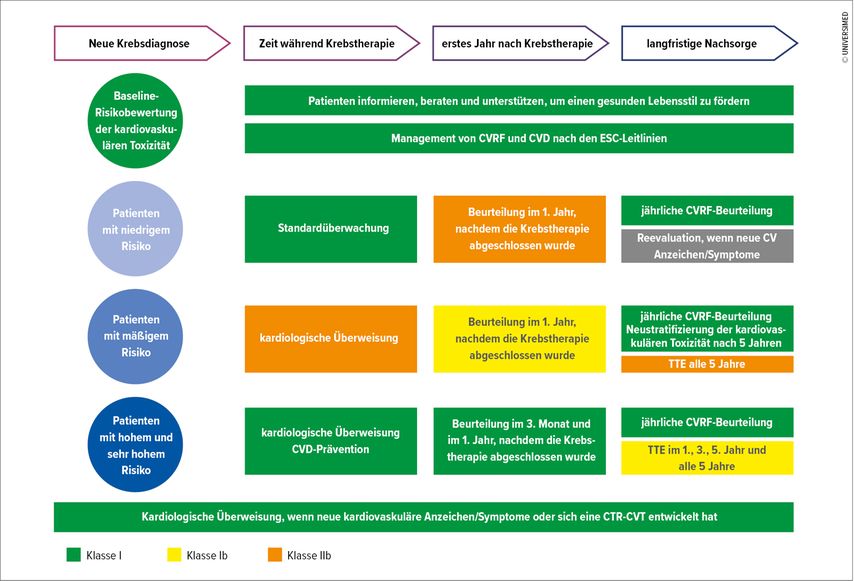
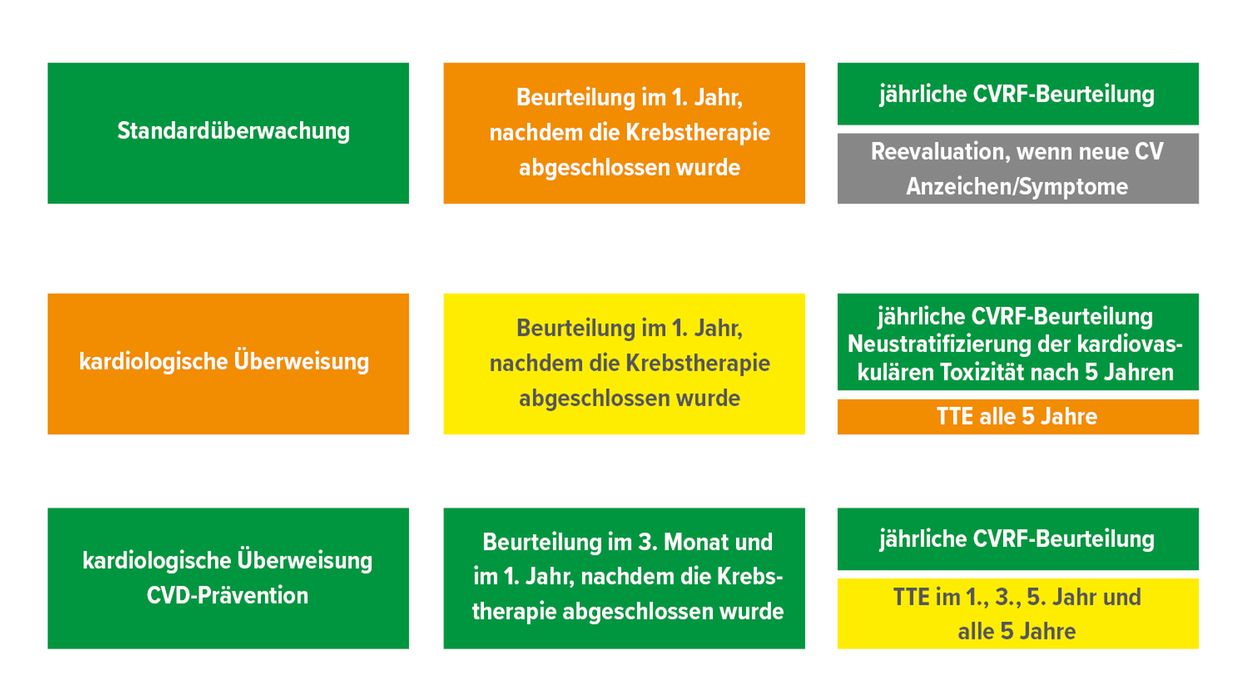
Um das individuelle Risiko in Abhängigkeit von der bevorstehenden Therapie abschätzen zu können, wurde mit den HFA-ICOS-Risk-Assessment-Tools ein Score zur Quantifizierung dieses Risikos eingeführt (Abb. 1). Neben dem EKG wird für alle Patienten ein Herzultraschall (vorzugsweise 3D-Echokardiografie) empfohlen. Mittels „global longitudinal strain“ (GLS) soll die linksventrikuläre Globalfunktion bestimmt werden. Die genannten Untersuchungen erlauben eine Einteilung der Patienten in die Risikogruppen „niedrig“, „moderat“ und „hoch“. Diese Einstufung soll von den Onkologen bei der Therapieplanung berücksichtigt werden.
Abb. 1: Kardioonkologische Behandlungsalgorithmen nach dem HFA-ICOS-Risikobewertungstool (modifiziert nach Lyon AR et al. 2022)1
Während der onkologischen Therapie wird zwischen primärpräventiven Maßnahmen für Herzgesunde und Sekundärprävention für kardial vorerkrankte Patienten unterschieden. In der Prävention können verschiedene in der Kardiologie gut bekannte Substanzklassen wie ACE-Inhibitoren, Statine, Betablocker und dergleichen eingesetzt werden. Für die verschiedenen Klassen onkologischer Therapie werden detaillierte Empfehlungen zum Monitoring während der Therapie und für das Jahr danach gegeben. Dies gilt in leicht abgewandelter Form auch für die Strahlentherapie.
Behandlungsalgorithmen für jede Klasse onkologischer Medikamente
Hinsichtlich des Managements kardiovaskulärer Toxizitäten betont die Leitlinie, dass sich dieses zum Teil vom Management kardialer Erkrankungen bei Patienten ohne Krebserkrankung unterscheidet. So sollten Therapieentscheidungen unter anderem die Lebenserwartung des Patienten sowie die Symptomlast und die Patientenpräferenzen berücksichtigen. Hinsichtlich möglicher Medikamenteninteraktionen liefert die Leitlinie umfassendes Tabellenmaterial. Für das Management kardialer Toxizitäten werden zu jeder Klasse onkologischer Therapien komplette Algorithmen zur Verfügung gestellt, die unter anderem die Ausprägung der Toxizität sowie die Symptomatik in Betracht ziehen. Diese Algorithmen legen auch fest, wann eine Therapie wegen nicht akzeptabler Toxizität unterbrochen oder abgebrochen werden muss. Das Problem der Verlängerung der QT-Zeit unter onkologischen Therapien wird in einem eigenen Kapitel abgehandelt. Eigene Abschnitte gibt es auch zur Antikoagulation und zum Management von Hypertonie.
Was folgt nach der Beendigung der onkologischen Therapie?
Nach Beendigung der onkologischen Therapie wird eine weitere Risikobewertung empfohlen, bei der die Wahrscheinlichkeit erhoben wird, dass es in Zukunft zum Auftreten einer kardialen Erkrankung kommt. Musste im Verlauf der Krebstherapie auch eine Therapie einer neu aufgetretenen Herzinsuffizienz begonnen werden, so legt die Leitlinie fest, wie diese Patienten überwacht werden sollen und ob ein Absetzen der Therapie möglich wird. Handelt es sich um eine schwere Herzinsuffizienz, wird eine lebenslange Behandlung dieser Herzinsuffizienz empfohlen. Handelt es sich um eine leichte oder moderate Herzinsuffizienz, kann bei entsprechendem Monitoring ein Absetzen der Therapie möglich werden.
Bei Langzeitüberlebenden von Krebserkrankungen wird auch ein langfristiges kardiologisches Monitoring empfohlen, das zumindest jährlich stattfinden und einfache Parameter wie Blutdruck und Plasmalipide umfassen sollte. In Abhängigkeit vom individuellen Risiko können weitere Untersuchungen wie der Herzultraschall hinzukommen. Hinsichtlich des langfristigen Managements werden detaillierte Empfehlungen in Abhängigkeit von der konkreten, aufgetretenen Komplikation (Hypertonie, Herzinsuffizienz, Myokarditis etc.) gegeben. Empfehlungen gibt es auch für spezielle Patientengruppen, wie zum Beispiel Personen mit kardialen Tumoren oder für die Durchführung von Strahlentherapie bei Patienten, die implantierte kardiale Devices tragen.
Literatur:
1 Lyon AR et al.: 2022 ESC Guidelines on cardio-oncology developed in collaboration with the European Hematology Association (EHA), the European Society for Therapeutic Radiology and Oncology (ESTRO) and the International Cardio-Oncology Society (IC-OS). Eur Heart J 2022; ehac244
Das könnte Sie auch interessieren:
Hinweise auf schlechteren Verlauf bei Männern bestätigt
Obwohl Frauen häufiger an einer Lupusnephritis erkranken, scheint diese bei Männern schwerer zu verlaufen. Diese Hypothese wird von einer Metaanalyse der Universität Minnesota unterstützt.1 Männer bekamen häufiger eine Nephritis vom Grad IV ± V, hatten schlechtere Nierenparameter und eine geringere Wahrscheinlichkeit für eine komplette Remission.
L’élastographie hépatique
En hépatologie, l’élastographie hépatique est l’instrument central de la prise en charge des patient·es atteint·es d’une maladie hépatique chronique. Les nouvelles conclusions permettent ...
Risques du tabagisme pour la santé – sevrage tabagique
«Un fumeur avide qui lit et relit l’importance des risques du tabagisme pour sa santé cesse dans la plupart des cas ... de lire», avait déclaré Winston Churchill. «Le tabac est le seul ...