Therapie der NASH: Phase-II-Daten machen Hoffnung
Bericht:
Reno Barth
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Ungeachtet ihrer Häufigkeit und klinischen Bedeutung gibt es für die nichtalkoholische Fettlebererkrankung (NAFLD) und die nichtalkoholische Steatohepatitis (NASH) bis dato keine zugelassenen Therapien. Im Rahmen des virtuellen Kongresses der American Association for the Study of Liver Diseases (AASLD) wurden mehrere Studien zur Therapie von NAFLD/NASH vorgestellt und beim „Wrap-Up Hepatologie“ von einer heimischen Expertin kommentiert.
In klinischen Studien zur Indikation nichtalkoholische Steatohepatitis (NASH) befinden sich aktuell zahlreiche Kandidaten, so Univ.-Prof. Dr. Petra Munda von der Wiener Universitätsklinik für Innere Medizin III, die auch anmerkt, dass in den letzten Jahren bereits einige Substanzen im Verlauf des klinischen Entwicklungsprogramms gescheitert sind. Histologische Endpunkte dieser Studien sind unter anderem die Abheilung der NASH ohne Zunahme der Fibrose bzw. die Abnahme der Fibrose ohne Zunahme der NASH, Reduktion der Entzündung sowie idealerweise die Abheilung (Resolution) der NASH in Kombination mit einer Verbesserung der Fibrose um mindestens eine Stufe. Die Erhebung aller dieser Endpunkte erfordert allerdings eine Leberbiopsie, was die Rekrutierung von Studienpatienten erheblich erschwert. Daher werden dringend nichtinvasive Parameter gesucht, die den Zustand der Leber verlässlich repräsentieren. Dies kann beispielsweise der mittels MRT bestimmbare Fettgehalt der Leber sein. Typische sekundäre Endpunkte in Studien sind Leberenzymwerte und der mit dem Fibroscan gemessene Fibrosegrad.
GLP-1-Rezeptor-Agonist mit günstigem Lebereffekt
Eine Substanz, die aktuell in der Indikation NASH evaluiert wird, ist das aus der Diabetestherapie bekannte GLP-1-Analogon Semaglutid (Sema). Generell gelten die GLP-1-Agonisten schon seit längerer Zeit als Hoffnungsträger in der Behandlung von NAFLD/NASH, so Munda. Diese Erwartungen seien nicht zuletzt durch die Ergebnisse der mit Liraglutid durchgeführten LEAN-Studie geweckt worden und beruhen auf den pleiotropen Wirkungen dieser Substanzgruppe, die einige Effekte auf die Leber inkludieren wie die Reduktion der endogenen Glukoseproduktion, der De-novo-Lipogenese und der Lipotoxizität, sowie Verbesserung der Insulinsensitivität der Leber. Der mit dem GLP-1-Rezeptor-Agonisten (GLP-1RA) erreichte Gewichtsverlust sollte ebenso zu einer Besserung der NASH beitragen.
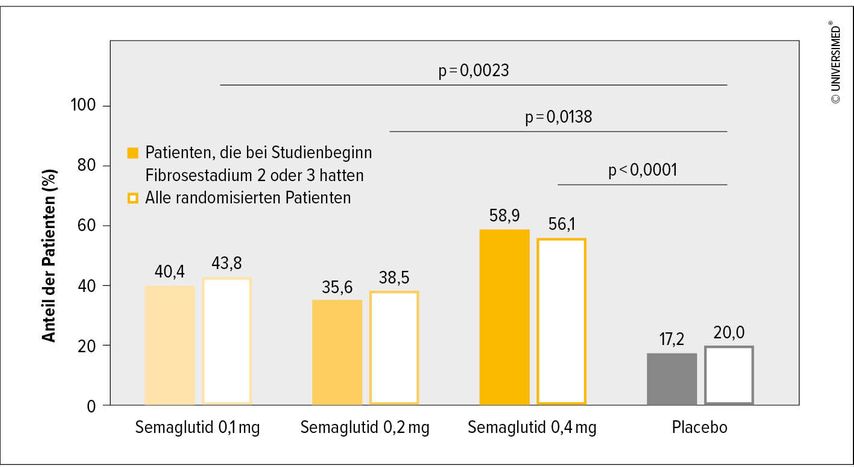
Im Rahmen des AASLD-Kongresses wurden nun Ergebnisse einer Phase-II-Studie vorgestellt, die drei unterschiedliche Dosierungen von Semaglutid im Vergleich zu Placebo untersuchte.1 Die Patienten litten unter bioptisch verifizierter NASH mit Fibrosegrad F1–F3, einem NAFLD Activity Score (NAS) ≥4 und einem Body-Mass-Index (BMI) >25kg/m2 und erhielten randomisiert täglich 0,1, 0,2 oder 0,4mg Sema oder Placebo subkutan über 72 Wochen. Biopsien wurden zu Beginn und am Ende der Studie durchgeführt. Primärer Endpunkt war die Abheilung der NASH ohne Zunahme der Fibrose, Verbesserung der Fibrose ohne Zunahme der NASH wurde als konfirmatorischer sekundärer Endpunkt erhoben. Von den insgesamt 320 Patienten gingen 230 mit Fibrosegrad F1–F3 in die Auswertung ein. Sema erwies sich in allen drei Dosierungen im Vergleich zu Placebo als überlegen. Der primäre Endpunkt wurde in den drei Verumgruppen von 40,4%, 35,6% bzw. 58,9% und in der Placebogruppe von 17,2% der Patienten erreicht (p<0,05 für alle Dosierungen) (Abb. 1). Hinsichtlich des konfirmatorischen sekundären Endpunktes zeigte sich ein ganz ähnliches Bild. Unter Sema verbesserten sich auch alle Komponenten des NAS. Eine Verschlechterung der Fibrose war unter Semaglutid seltener als unter Placebo. Je nach Dosis kam es zu einer Verbesserung der Fibrose zwischen 30 und 49%, jedoch war die Placeboantwort hinsichtlich der Fibrose so deutlich, dass in diesem Endpunkt die Signifikanz verfehlt wurde. Erwartungsgemäß nahmen die Patienten in den Sema-Gruppen um bis zu 12,5% ab. Das HbA1c verbesserte sich ebenso wie die Leberwerte (Transaminasen) und verschiedene Parameter des Lipidstoffwechsels (HDL, Triglyzeride).1
Abb. 1: Abheilung der Steatohepatitis und keine Verschlechterung der Leberfibrose (modifiziert nach Newsome P et al. 2020)1
Lanifibranor: breiter Angriff auf die PPA-Rezeptoren
Ebenfalls neue Daten gibt es zu dem pan-Peroxisom-Proliferator-aktivierten(PPA)Rezeptor-Agonisten Lanifibranor, der auf die PPA-Rezeptoren alpha, gamma und delta wirkt. In der nun präsentierten Studie wurden zwei Dosierungen von Lanifibranor über 24 Wochen verglichen.2 Munda weist darauf hin, dass bei dieser Studie ein anderer Endpunkt verwendet wurde als in den Studien mit Semaglutid, nämlich eine Veränderung des SAF-Activity-Scores um mindestens zwei Punkte. Damit liegt der Fokus der Studie auf der entzündlichen Aktivität in der Leber. Dazu passend war eine nicht zirrhotische, aber hochaktive NASH mit einem SAF-Activity-Score von 3–4 ein Einschlusskriterium. NASH-Abheilung und Regression der Fibrose waren sekundäre Endpunkte. In der Dosierung von 1200mg am Tag erreichte Lanifibranor nach der relativ kurzen Beobachtungszeit von 24 Wochen den primären und alle sekundären Endpunkte. Zu einer Abnahme des SAF um mindestens zwei Punkte kam es in der 1200mg-Gruppe bei 49% der Patienten, NASH-Abheilung ohne Zunahme der Fibrose erreichten nach 24 Wochen 45% der Patienten. Der kombinierte sekundäre Endpunkt aus NASH-Abheilung und Besserung der Fibrose trat unter Lanifibranor 1200mg bei 31% der Patienten ein. Lanifibranor wurde sehr gut vertragen, was sich nicht zuletzt in einer Drop-out-Rate von unter 5%äußerte. Bei Patienten mit Diabetes nahm das HbA1c um mehr als 0,5% ab. In beiden Verumgruppen nahmen die Triglyzeride ab und das HDL-Cholesterin stieg. Als Nachteil der Therapie zeigte sich unter Lanifibranor eine dosisabhängige Gewichtszunahme von 2,4 bzw. 2,7kg, während Placebopatienten kein Gewicht zulegten.2
Neue Ziele und neue Substanzen: FGF-Analoga in Studien
Auf einem gänzlich anderen Wirkmechanismus basiert Aldaferin, ein Analogon des im Ileum ausgeschütteten Hormons FGF19 („fibroblast growth factor 19“), das die Synthese von Gallensäuren inhibiert und die metabolische Homöostase reguliert. Im Rahmen des AASLD-Kongresses 2020 wurden die Ergebnisse einer 24-wöchigen Phase-II-Studie zu Aldaferin in der Indikation NASH präsentiert.3 Primärer Endpunkt war der aus der Biopsie bestimmte absolute Fettgehalt der Leber. Munda weist darauf hin, dass in Vorstudien unter Aldaferin ein Anstieg des LDL-Cholesterins beobachtet wurde, weshalb in der aktuellen Studie eine Verabreichung von Rosuvastatin im Studiendesign inkludiert war. Wurde zu Woche 2 ein LDL-Anstieg um mindestens 10mg beobachtet, so musste die Statintherapie initiiert werden. Aldaferin reduzierte in 24 Wochen den absoluten Leberfettgehalt um 7,7%. Dies sei, so Munda, eine „eindrucksvolle Reduktion“ und entspreche einer relativen Abnahme des Leberfetts um 38,8%. Dementsprechend deutlich waren auch die Ergebnisse bei den sekundären Endpunkten. So kam es bei 22% der Patienten sowohl zu einer Abheilung der NASH als auch zu einer Verbesserung der Fibrose. In der Placebogruppe wurde dieser Endpunkt von keinem einzigen Patienten erreicht. Leberwerte und Entzündungsparameter verbesserten sich unter Aldaferin ebenfalls. Dieser deutlichen Wirksamkeit stand als unerwünschte Wirkung vor allem der Anstieg des LDL-Cholesterins gegenüber, der dazu führte, dass 96% der Patienten Rosuvastatin benötigten. Sollte Aldaferin die Zulassung erhalten, werde man es, so Munda, wohl als Kombinationstherapie mit Rosuvastatin sehen müssen. Man könne davon ausgehen, dass die Phase III bereits so geplant wird.3
Eine weitere Substanz, die bei einem der FGF-Hormone ansetzt, ist das FGF21-Analogon Efruxifermin (EFX), ein Fusionsprotein aus humanem IgG1 Fc und FGF21. In der Indikation NASH befindet sich Efruxifermin in der Phase IIa, Ergebnisse einer Studie mit 80 Patienten, die über 16 Wochen subkutanes EFX in den Dosierungen 28mg, 50mg und 70mg oder Placebo erhielten, wurde ebenfalls im Rahmen des AASLD-Kongresses vorgestellt.4 Primärer Endpunkt war die Reduktion des mittels MRT bestimmten Leberfetts zu Woche 12. Patienten, bei denen eine Reduktion des Leberfetts von mindestens 30% beobachtet wurde, unterzogen sich zu Woche 16 zwecks Bestätigung des Resultats einer Biopsie. Der primäre Endpunkt wurde mit allen Dosierungen von EFX erreicht. Nach Woche 12 zeigten 50 von 80 Patienten eine relative Reduktion des Leberfetts von mindestens 30% und waren damit Kandidaten für die Biopsie. Nach 16 Wochen wurde bei 48% des Studienkollektivs eine Verbesserung der Fibrose um mindestens einen Grad ohne Verschlechterung der NASH festgestellt. Eine Abheilung der NASH ohne Verschlechterung der Fibrose zeigten ebenfalls 48%, und 28% erreichten eine Verbesserung der Fibrose um mindestens zwei Grade.4
Zusätzlich lieferte die Studie Hinweise auf eine Reihe weiterer günstiger Effekte von EFX wie einer Triglyzeridsenkung, einer HDL-Erhöhung ohne Anstieg des LDL sowie einer Reduktion des HbA1c (unter den Dosierungen 50 und 70mg). In allen Dosisgruppen wurde jedoch eine Abnahme des C-Peptids registriert, was auf eine geringere Insulinausschüttung infolge verbesserter Insulinsensitivität schließen lässt. Häufigste Nebenwirkungen waren transiente, milde oder moderate gastrointestinale Symptome.4
Nicht zuletzt zeigte eine Proof-of-Concept-Studie mit dem „small molecule“ TVB-2640 als erster Vertreter der neuen Klasse der Fettsäure-Synthese-Inhibitoren einen deutlichen Effekt auf den Fettgehalt der Leber.5
Quelle:
„Neue Therapien bei NASH/NAFLD“, Vortrag von Ao. Univ.-Prof. Dr. Petra Munda, Wien, im Rahmen des „Wrap-Up Hepatologie AASLD/EASL 2020“; onlineWEBseminar vom 9. Jänner 2021
Literatur:
1Newsome P et al.: AASLD 2020; Abstract No. 10 2 Francque SM et al.: AASLD 2020; Abstract No. 12 3 Harrison SA et al.: AASLD 2020; Abstract No. 72 4 Harrison SA et al.: AASLD 2020; Abstract No. 85 5 Loomba R et al.: AASLD 2020; Abstract No. 67
Das könnte Sie auch interessieren:
HIV-Diagnostik: Die Unterstützung vonseiten der Dermatologie ist gefragt!
Etwa 40% der HIV-Erstdiagnosen in Österreich werden zu einem Zeitpunkt gestellt, zu welchem das Immunsystem der Patient:innen bereits stark beeinträchtigt ist.1 Solche späten Diagnosen ...
Vitiligo: mit Ausdauer und Kombinationstherapien zum Erfolg
Rasche Diagnosesicherung und Therapieeinleitung sind bei der Vitiligo essenziell, auch aufgrund der individuellen Belastungssituation vieler Patient:innen. Vier Therapieziele, die ...
Periphere Nervenscheidentumoren
Periphere Nervenscheidentumoren sind eine seltene, aber dennoch bedeutende Tumorentität, die das periphere Nervensystem betrifft. Sie können eine Vielzahl an Symptomen verursachen und ...