Die delaminierte Rotatorenmanschette
Autoren:
DDr. Jakob E. Schanda1,2,3,4
Univ.-Prof. Dr. Christian Fialka, MBA1,5
Priv.-Doz. Dr. Philipp R. Heuberer6,7
1 AUVA Traumazentrum Wien, Standort Meidling
2 LBI für Traumatologie, Wien
3 Austrian Cluster for Tissue Regeneration, Wien
4Michael-Ogon-Labor für Orthopädische Forschung, Orthopädisches Spital Speising, Wien
5 Sigmund Freud Privatuniversität Wien, Fakultät für Medizin, Zentrum für den Bewegungsapparat
6 healthPi Medical Center, Wien
7 Austrian Research Group for Regenerative and Orthopedic Medicine (AURROM), Wien
Korrespondierender Autor:
DDr. Jakob E. Schanda
E-Mail: jakob.schanda@auva.at
Eine Sehnendelamination wird bei bis zu 90% aller chronischen Rotatorenmanschettenrupturen beobachtet. Mittels Magnetresonanztomografie ist eine Sehnendelamination nur unzureichend erkennbar – allerdings sind chronisch delaminierte Rotatorenmanschettenrupturen mit einer fortgeschrittenen medialen Sehnenretraktion und einer vermehrten fettigen Muskelinfiltration vergesellschaftet.
Keypoints
-
Das Erkennen einer Sehnendelamination ist entscheidend, da eine Rekonstruktion beider makroskopisch sichtbaren Sehnenschichten signifikant bessere klinische Ergebnisse sowie geringe Rerupturraten aufweist.
-
Eine individuelle Rekonstruktion beider Sehnenschichten führt zu biomechanisch stabileren Verhältnissen als eine „En masse“-Rekonstruktion, bei welcher beide Sehnenschichten auf einmal gefasst und rekonstruiert werden.
Epidemiologie von delaminierten Rotatorenmanschettenrupturen
Transmurale Rupturen der Rotatorenmanschette treten bei rund 20% der arbeitenden Bevölkerung über 50 Jahre auf.18,31 Bei rund 60% der Patienten über 80 Jahre werden degenerative Veränderungen der Rotatorenmanschette berichtet, wie eine mediale Retraktion des Sehnenstumpfs oder eine fettige Infiltration der Muskulatur bis hin zur Muskelatrophie.5,16,31
Mikroskopisch betrachtet besteht die Rotatorenmanschette aus fünf verschiedenen Schichten, welche durch eine unterschiedliche Verteilung und Anordnung von Muskel- und Sehnenfasern gekennzeichnet sind.4,20 Von diesen fünf verschiedenen Schichten lassen sich makroskopisch jedoch nur zwei unterscheiden.4 Die oberflächliche bursaseitige Schicht stellt die eigentliche flexiblere Sehne dar, während die tiefer liegende ligamentäre Schicht die steifere glenohumerale Gelenkkapsel ist.17,21,29
Je nach Definition der Sehnendelamination wird ihre Inzidenz im Rahmen von Rotatorenmanschettenrupturen mit 38–92% angegeben.1,2,6,15,28,30 Han et al. berichteten über eine Sehnendelamination von 88% bei posterioren und 42% bei anterioren Rotatorenmanschettenrupturen.6 Die Autoren gaben jedoch nicht an, welche Sehnen genau betroffen waren. In einer eigenen Untersuchung, in welcher arthroskopische Bilder mit Magnetresonanztomografiebefunden von 349 Schultern verglichen wurden, konnten wir eine Sehnendelamination bei 66,2% im Rahmen von chronischen Rotatorenmanschettenrupturen beobachten, jedoch mit einem signifikanten Unterschied in der Verteilung je nach zugrunde liegendem Muster der Rotatorenmanschettenruptur.25 Ähnlich der Studie von Han et al. beobachteten wir eine Sehnendelamination am häufigsten (84,6%) bei postero-superioren Rotatorenmanschettenrupturen mit Beteiligung der Supraspinatus- und Infraspinatussehne. Bei antero-superioren Rotatorenmanschettenrupturen mit Beteiligung der Supraspinatus- und Subscapularissehne konnten wir eine Sehnendelamination bei 57,7% beobachten.25
Kürzlich berichteten Boileau et al. über eine zunehmende Sehnendelamination bei größeren Rotatorenmanschettenrupturen mit fortgeschrittener medialer Sehnenretraktion.1 In ähnlicher Weise beobachteten wir in unserer Untersuchung eine signifikante Zunahme der Sehnenretraktion bei Patienten mit Rotatorenmanschettendelamination.25 Weiters haben wir beim Vergleich verschiedener Rupturmuster signifikante Unterschiede bei der medialen Sehnenretraktion zwischen delaminierten und nicht delaminierten Rotatorenmanschettenrupturen festgestellt: Multivariate Regressionsanalysen zeigten signifikante Zusammenhänge zwischen der Retraktion der Supraspinatus- und der Infraspinatussehne und dem Vorhandensein einer Rotatorenmanschettendelamination.25
In unserer Studie konnten wir signifikanten Unterschiede hinsichtlich der fettigen Muskelinfiltration des Supraspinatus und Infraspinatus zwischen delaminierten und nicht delaminierten Rotatorenmanschettenrupturen beobachten. Außerdem wurden signifikante Unterschiede in der fettigen Muskelinfiltration des Supraspinatus, des Infraspinatus und des Subscapularis beim Vergleich verschiedener Rupturmuster zwischen delaminierten und nicht delaminierten Rotatorenmanschettenrupturen festgestellt.25 Da die fettige Muskelinfiltration in engem Zusammenhang mit der Rupturgröße und -lokalisation steht, welche typischerweise bei chronischen Rotatorenmanschettenrupturen beobachtet werden,12 muss die Sehnendelamination ebenfalls als Befund chronischer Rotatorenmanschettenrupturen interpretiert werden.
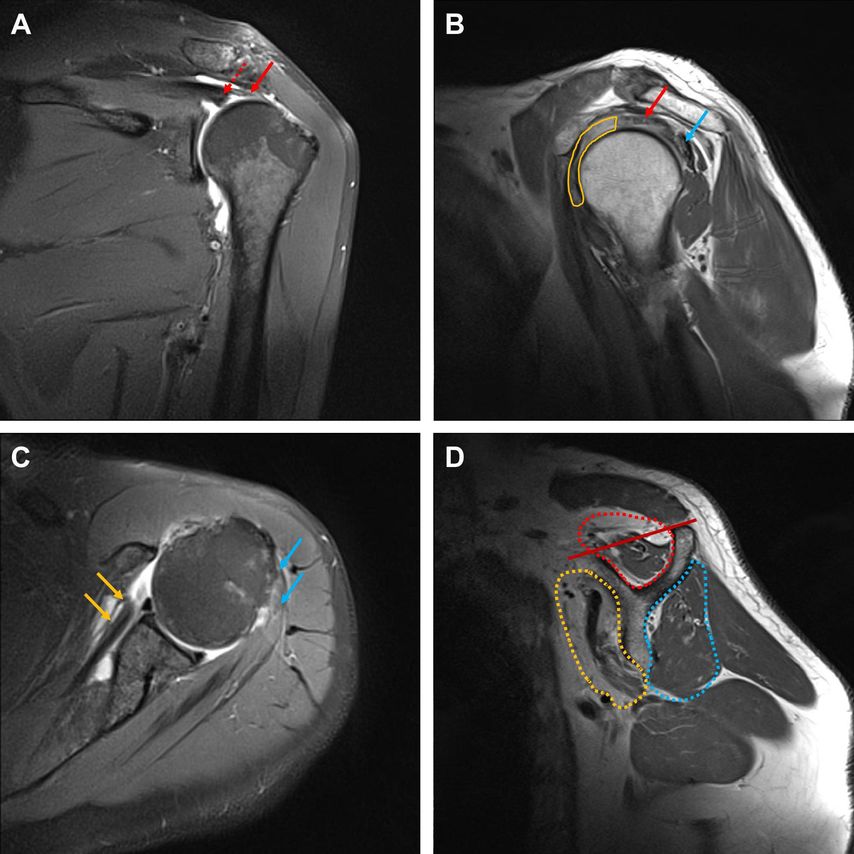
Nur wenige Arbeiten befassten sich mit der Detektion einer Sehnendelamination bei Rotatorenmanschettenrupturen. Eine Studie untersuchte die Genauigkeit der Sehnendelamination der Rotatorenmanschette anhand einer Magnetresonanzarthrografie.3 Bei insgesamt 231 Schultern mit Rupturen der Supraspinatus- und Infraspinatussehne berichteten die Autoren über eine Sensitivität von 86 bis 100% sowie eine Spezifität von 82 bis 100%, abhängig vom Ausmaß der Sehnenretraktion.3 Da eine Magnetresonanzarthrografie invasiver, zeitaufwendiger und teurer als eine konventionelle Magnetresonanztomografie ist, wird Erstere nicht routinemäßig für die Diagnose von Rotatorenmanschettenrupturen durchgeführt.14 Unsere Untersuchung an 349 Schultern stellte eine geringe Sensitivität von 35,5%, jedoch eine ausgezeichnete Spezifität von 100% der Magnetresonanztomografie für die Detektion einer Sehnendelamination fest.25 Aber auch wenn in der Magnetresonanztomografie keine Sehnendelamination sichtbar ist, können eine fortgeschrittene Sehnenretraktion und eine stärkere fettige Muskelinfiltration einen Hinweis auf das Vorhandensein einer Sehnendelamination geben (Abb.1). Wurde in der Magnetresonanztomografie eine Sehnendelamination festgestellt, wiesen die Patienten eine signifikant stärkere mediale Sehnenretraktion sowie einen höheren Anteil an fettiger Muskelinfiltration des Supraspinatus und Infraspinatus auf.25
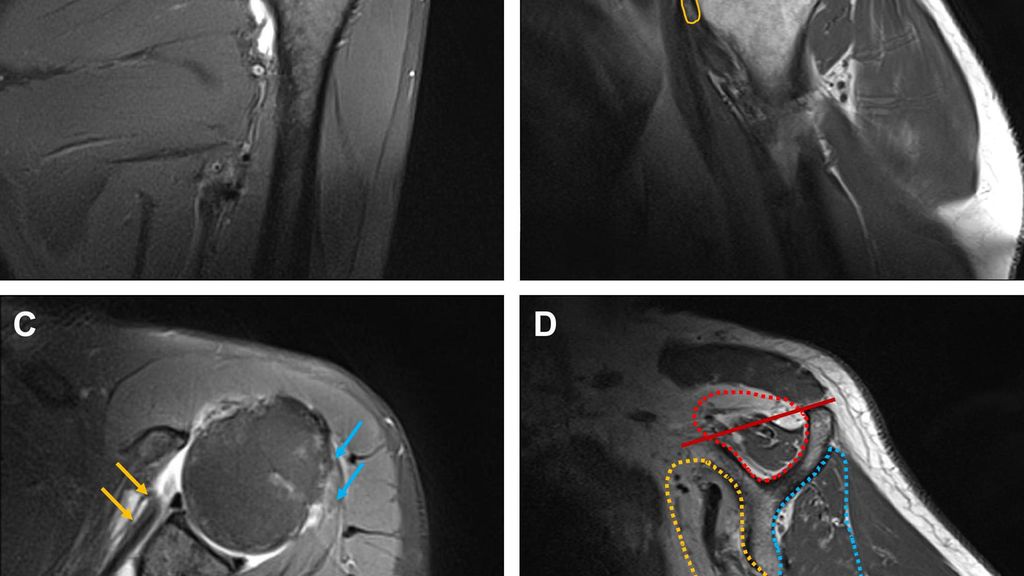
Abb. 1: MRT einer linken Schulter, transmurale Ruptur der Supraspinatus- und Subscapularissehne, Ansatztendinopathie der Infraspinatussehne. A) Coronale Schichtung; die Delamination der Supraspinatussehne ist klar sichtbar. Die oberflächliche Sehnenschicht ist bis auf Höhe des Humeruskopfs retrahiert (roter Pfeil), die tiefe Sehnenschicht ist noch weiter nach medial retrahiert (rot gepunkteter Pfeil). B) Parasagittale Schichtung; der posteriore Anteil der oberflächlichen Sehnenschicht des Supraspinatus zeigt intratendinöse Teilrupturen (roter Pfeil). Die Infraspinatussehne zeigt eine Ansatztendinopathie mit Flüssigkeitseinlagerungen (blauer Pfeil). Die antero-superiore Rotatorenmanschette mit der anterioren Supraspinatussehne und der Subscapularissehne ist nicht erkennbar im Sinne einer kompletten Ruptur (gelbes Areal). C) Axiale Schichtung; der kraniale Anteil der Subscapularissehne ist zur Gänze rupturiert und bis auf Höhe der anterioren Glenoidkante nach medial retrahiert (gelbe Pfeile). Die Infraspinatussehne zeigt eine Ansatztendinopathie mit Flüssigkeitseinlagerungen (blaue Pfeile). D) Parasagittale Schichtung; fettige Infiltration des Supraspinatus entsprechend Goutallier III (rot gepunktetes Areal) mit positiven Tangentenzeichen (dunkelroter Strich), fettige Infiltration des Subscapularis entsprechend Goutallier IV (gelb gepunktetes Areal), fettige Infiltration des Infraspinatus entsprechend GoutallierI (blau gepunktetes Areal)
Therapie von delaminierten Rotatorenmanschettenrupturen
Bislang lag der Fokus bei der Rotatorenmanschettenrekonstruktion hauptsächlich auf der Wiederbefestigung der nach medial retrahierten Sehne an ihren Footprint. Die Visualisierung und Rekonstruktion von beiden makroskopisch sichtbaren Sehnenschichten sind jedoch entscheidend für die strukturelle Integrität der Rotatorenmanschette.9,13 Moderne Rekonstruktionstechniken befassen sich daher mit der individuellen Rekonstruktion beider Sehnenschichten.7,8,11,19,30 Die zweischichtige, doppelreihige Rotatorenmanschettenrekonstruktion, bei welcher beide Sehnenschichten individuell und doppelreihig rekonstruiert werden, oder eine konventionelle „En masse“-Rekonstruktion, bei der die gesamte Sehnensubstanz in einer weniger anatomischen Art rekonstruiert wird, zeigen vergleichbare klinische Ergebnisse sowie Rerupturraten.13 Die moderne zweischichtige, doppelreihige Rekonstruktion führt jedoch postoperativ aufgrund der Vermeidung von nicht physiologischen Spannungsverhältnissen im Sehnengewebe zu signifikant weniger Schmerzen.13
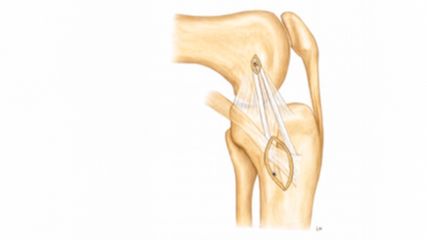
Eine neue Operationstechnik für die individuelle Rekonstruktion beider Sehnenschichten mithilfe eines knotenlosen transossären Äquivalents (Abb.2) bietet biomechanische Vorteile gegenüber einer medial verknoteten Rekonstruktion und knotenlosen transossären Äquivalenten ohne Berücksichtigung der delaminierten Sehne.11,24 Diese biomechanischen Vorteile erklären sich durch die spezielle Konfiguration und die damit verbundenen selbstverstärkenden Eigenschaften.22,23,26,27 Diese neue Operationstechnik wurde kürzlich mit einem medial verknoteten transossären Äquivalent bei delaminierten Rotatorenmanschettenrupturen verglichen. Hierbei konnte nach zwei Jahren gezeigt werden, dass die moderne Operationstechnik einen signifikant höheren Constant Score sowie eine verbesserte Abduktion und Anteversion bei vergleichbaren Rerupturraten liefert.10
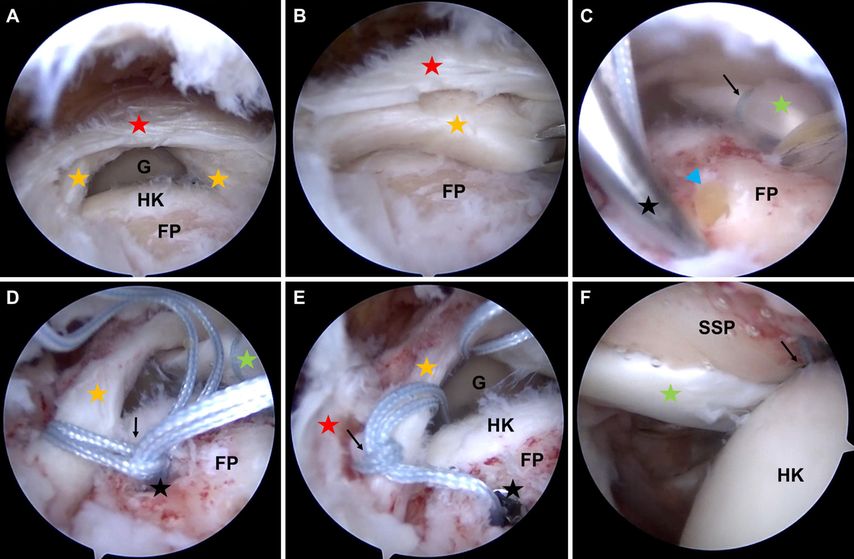
Abb. 2: Arthroskopie einer rechten Schulter, transmurale Ruptur der Supraspinatus- und Infraspinatussehne. A) Blick von lateral; der Humeruskopf (HK) mit dem Footprint (FP) der Supraspinatus- und Infraspinatussehne sowie das Glenoid (G) sind gut erkennbar. Es zeigt sich eine Delamination der postero-superioren Rotatorenmanschette wobei die tiefe Sehnenschicht (gelbe Sterne) weiter nach medial retrahiert ist als die darüber liegende oberflächliche Sehnenschicht (roter Stern). B) Blick von lateral; mit der Fasszange kann die tiefe Sehnenschicht (gelber Stern) an den FP reponiert werden und wird von der oberflächlichen Sehnenschicht (roter Stern) bedeckt. C) Blick von lateral; die lange Bizepssehne (grüner Stern) wurde als Augmentation am FP mittels spezieller Fadenankersysteme (schwarzer Pfeil) im Sinne einer modifizierten „superior capsule reconstruction“ fixiert. Um die Sehnenheilung zu fördern, wird mit einem 2mm-Bohrdraht (schwarzer Stern) der subchondrale Knochen angebohrt, um die Rekrutierung von stammzellhaltigem Knochenmark (blaues Dreieck) zu generieren. D) Blick von lateral; ein Fadenankersystem (schwarzer Stern) wurde im posterioren Anteil des Footprint (FP) eingebracht und zunächst die tiefer liegende Sehnenschicht (gelber Stern) mit einer Fadenschlinge (schwarzer Pfeil) armiert. Anterior ist die bereits zuvor fixierte lange Bizepssehne (grüner Stern) erkennbar. E) Blick von lateral; die zuvor durchgeführte Fadenschlinge (schwarzer Pfeil) des posterioren Fadenankers (schwarzer Stern) am Footprint (FP) des Humeruskopfs (HK) zur Armierung der tiefen Sehnenschicht (gelber Stern) wird in das Gelenk Richtung Glenoid (G) vorgelegt, um in weiterer Folge mit demselben Faden die oberflächliche Sehnenschicht (roter Stern) zu fixieren. F) Blick von posterior intraartikulär; der Humeruskopf (HK) ist zur Gänze mit der Rotatorenmanschette abgedeckt und die Ruptur verschlossen. Ein Faden (schwarzer Pfeil) ist im anterioren Anteil der Supraspinatussehne (SSP) erkennbar. Die lange Bizepssehne (grüner Stern) ist am oberen Glenoidrand sowie im anterioren Anteil des Humeruskopfs im Sinne einer modifizierten „superior capsule reconstruction“ fixiert
Literatur:
1 Boileau P et al.:Am J Sports Med 2019; 47(5): 1074-81 2 Boileau P et al.: J Bone Joint Surg Am 2005; 87-A(6): 1229-40 3 Choo HJ et al.: Am J Roentgenol 2015; 204(2): 360-6 4Clark JM, Harryman DTI: J Bone Joint Surg Am 1992; 74-A(5): 713-25 5 Codding JL, Keener JD:Curr Rev Musculoskelet Med 2018; 11(1): 77-85 6 Han Y et al.: Arthroscopy 2013; 29(11): 1740-7 7 Hepp P et al.: Arch Orthop Trauma Surg 2009; 129(8): 1031-6 8 Hepp P et al.: Am J Sports Med 2009; 37(7): 1363-9 9 Heuberer PR et al.: Am J Sports Med 2020; 48(3): 689-96 10 Heuberer PR et al.: Knee Surg Sports Traumatol Arthrosc 2019; 27(12): 3920-8 11 Heuberer PR et al.: Arthrosc Tech 2018; 7(1): e7-12 12 Kim HM et al.: J Bone Joint Surg Am 2010; 92-A(4): 829-39 13 Kim SJ et al.:Am J Sports Med 2016; 44(2): 468-7314 Liu F et al.: Orthop J Sports Med 2020; 8(2): 2325967119900356 15 MacDougal GA, Todhunter CR: J Shoulder Elbow Surg 2010; 19(7): 1063-9 16 Melis B et al.:Clin Orthop Relat Res 2010; 468(6): 1498-1505 17 Mihata T et al.: Am J Sports Med 2012; 40(10): 2248-55 18 Minagawa H et al.: J Orthop 2013; 10(1): 8-12 19 Mori D et al.: Arthrosc Tech 2014; 3(6): e667-71 20 Nakajima T et al.: J Shoulder Elbow Surg 1994; 3(2): 79-87 21 Nimura A et al.: J Shoulder Elbow Surg 2012; 21(7): 867-72 22 Park MC et al.: J Shoulder Elbow Surg 2014; 23(12): 1813-21 23 Park MC et al.: Arthroscopy 2017; 33(8): 1473-81 24 Pauzenberger L et al.: Am J Sports Med 2019; 46(13): 3165-73 25 Schanda JE et al.: Arthroscopy 2021; S0749-8063(21)01119-126. Online ahead of print 26 Smith GCS et al.: J Shoulder Elbow Surg 2017; 26(12): 2206-12 27 Smith GCS, Lam PH: Knee Surg Sports Traumatol Arthrosc 2018; 26(12): 3818-25 28 Sonnabend DH, Watson EM: J Shoulder Elbow Surg 2002; 11(3): 212-8 29 Sonnabend DH et al.:J Shoulder Elbow Surg 2001; 10(2): 109-15 30 Sugaya H et al.: J Bone Joint Surg Am 2007; 89-A(5): 953-60 31 Teunis T et al.: J Shoulder Elbow Surg 2014; 23(12): 1913-21
Das könnte Sie auch interessieren:
Frühe Unterwassertherapie nach totaler Hüft- und Knieendoprothese
Eine frühzeitige Durchführung der Unterwassertherapie mit wasserdichtem Folienverband ab dem vierten postoperativen Tag ist im Allgemeinen sicher, wirksam und ohne Nebenwirkungen.
Aktuelles zur anteromedialen Knieinstabilität
Kombinierte Verletzungen des medialen Kollateral- (MCL) und des vorderen Kreuzbandes (VKB) zählen zu den häufigsten multiligamentären Knieverletzungen. Bei vermeintlich isolierten VKB- ...
Arthroskopische Behandlung von Glenoidrandfrakturen
In der Literatur werden die Begriffe knöcherne Bankart-Läsion und Glenoidrandfraktur häufig synonym verwendet, obwohl sie sich hinsichtlich Pathomechanismus und Therapie deutlich ...