Stroke–„organization of care“
Autorin:
Prim. Univ.-Prof. Dr. Elisabeth Fertl
Abteilung Neurologie
Klinik Landstraße
Wien
In der Schlaganfallakutversorgung gibt es derzeit drei Behandlungssäulen, die in vielen Ländern bereits langjährig gelebte Routine sind: Es begann vor Jahrzehnten mit der Stroke-Unit-Behandlung, dann folgte die i.v. Thrombolyse von Gehirngefäßverschlüssen innerhalb eines Zeitfensters von 4,5 Stunden und zuletzt 2016 die Rekanalisation durch endovaskuläre Thrombektomie bei ausgewählten Patienten. Bekanntlich ist der Schlaganfall eine der häufigsten Todesursachen und die häufigste Ursache für Behinderung im Erwachsenenalter in Industrieländern.
Das vorrangige Behandlungsprinzip beim Schlaganfall lautet unverändert „time is brain“; ein Behandlungserfolg setzt also voraus, dass alle Teile der Behandlungskette kompetent und gut organisiert sind. Als Behandlungserfolg wird dabei ein Überleben ohne funktionell relevante Behinderung (modified RANKIN Scale 0–2 auf einer 7-stufigen Skala) definiert. Im Gegensatz zum Herzinfarkt verursacht ein Hirninfarkt üblicherweise keine Schmerzen, sodass der Notfall von Laien anhand von Leitsymptomen (z.B. schlagartige Sprachstörung, Halbseitenlähmung etc.) erkannt werden muss.
Dies erfordert laufend aktive Öffentlichkeitsarbeit und Schulung der Rettungssanitäter. Die Anpassung der Behandlungspfade an neue wissenschaftliche Erkenntnisse muss hingegen aktiv von den verschiedenen Verantwortlichen im Schlaganfallakutmanagement angestrebt werden. Hier werden nun einige aktuell wichtige Themen für die Organisation der Schlaganfallversorgung in Österreich beschrieben.
In Österreich wurde bereits 1997 mit Etablierung der LKF-Krankenhaus-Abrechnung dem prozesshaften Verlauf des Schlaganfallmanagements Rechnung getragen. Für die Frührehabilitation nach einem Schlaganfall im Krankenhaus wurden bereits 1997 Struktur- und Prozessqualitätskriterien definiert, ohne deren Erfüllung keine Abrechnung erfolgen kann. Ebenso gibt es mit 38 Stroke Units und mehreren regionalen Interventionszentren ein dichtes stationäres Versorgungsnetz für die österreichische Bevölkerung von >8 Mio. Einwohnern. Dennoch sind für Stroke Units bis 2030 Erweiterungen der Bettenkapazität aufgrund der steigenden Inzidenz akuter Schlaganfälle geplant.
Auch der Bereich der Schlaganfallrehabilitation außerhalb des LKF-Systems ist national gut ausgebaut, an diversen Schnittstellen findet sich jedoch immer wieder Adaptationsbedarf. Es gibt bereits mehrere bewährte nationale Maßnahmen der Qualitätssicherung in der Schlaganfallversorgung:
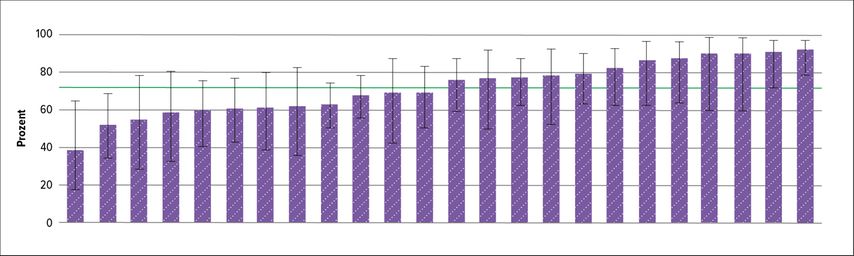
Das österreichische Stroke-Unit-Register (ASUR=Austrian Stroke Unit Registry) besteht seit 2005 und wird von der Gesundheit Österreich GmbH im Bundesinstitut für Qualität im Gesundheitswesen als nationales webbasiertes Qualitätsregister geführt. In Zusammenarbeit mit der ÖGSF (Österreichische Gesellschaft für Schlaganfallforschung) haben sich alle Stroke-Unit-Betreiber in Österreich geeinigt, einen umfangreichen Datensatz für jeden Schlaganfallpatienten, der an einer Stroke Unit behandelt wird, einzugeben. Eine Datenerfassung erfolgt bei Aufnahme und Entlassung aus der Stroke Unit sowie bei einem ambulanten Nachsorgetermin etwa 3 Monate nach dem Ereignis. Jedes Jahr werden mehr als 15000 Datensätze eingegeben. Es erfolgt ein automatisiertes Benchmarking für jede Stroke Unit, wobei jährlich die eigenen Ergebnisse mit denen aller anderen Stroke Units verglichen werden. So kann man bei wesentlichen Qualitätsparametern (z.B. Lyse-Rate bei ausgewählten Patienten: Anteil der Pat. <80 Jahren mit zerebraler Ischämie und definiertem Schweregrad, die im Zeitfenster das Krankenhaus erreichen) etwa das eigene Leistungsvolumen mit dem anderer Stroke Units in Beziehung stellen und eventuell notwendige Organisationsänderungen veranlassen (Abb. 1).
Abb. 1: GÖG-Register: Lyserate an Stroke Units in Österreich 2020 bei ausgewählten Patienten (Ischämie, Alter <80 Jahren, NIHSS >3, Ankunft im Krankenhaus <3,5 Stunden; grüne Linie = Mittelwert in Österreich)
Diese Daten sind auch datenschutzkonform pseudonymisiert und mit dem österreichischen Sterberegister verknüpft, sodass Patientenkarrieren nachverfolgt werden können. Neben der Qualitätsüberprüfung individueller Stroke Units können somit auch nationale Trends in der Akutversorgung von Schlaganfällen über die Jahre belegt werden. Diese Datenbasis unterstützt also die Gesundheitsplanung wesentlich. Außerdem sind zahlreiche wissenschaftliche Publikationen aus dieser Datenbank entstanden, die eine führende Rolle Österreichs in vielen Aspekten der Schlaganfallversorgung belegen.
Entsprechend den Zielen der ESO (European Stroke Organisation) sollen in Europa bis 2030 etwa 90% aller Schlaganfallpatienten auf Stroke Units behandelt werden. Gleichzeitig soll durch konsequente vaskuläre Präventionsmaßnahmen die Inzidenz von Schlaganfällen um 10% gesenkt werden. Jedes europäische Land sollte einen „Schlaganfallbehandlungspfad“ definieren, um den oben erwähnten vielgliedrigen Versorgungsprozess nachhaltig zu standardisieren.
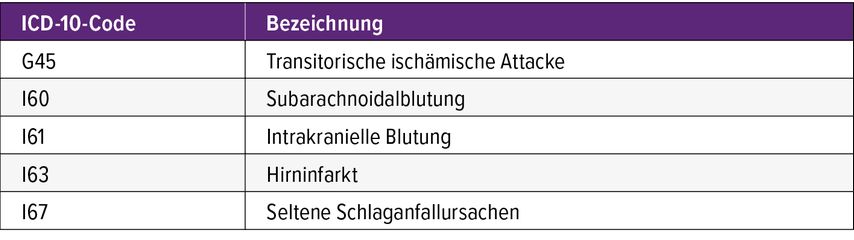
Seit 2013 gibt es parallel zum GÖG-Stroke-Register auch die nationale Qualitätsstrategie des A-IQI (Austrian Inpatient Quality Index) über das Bundesministerium für Gesundheit. Hier wird unter Nutzung von LKF-Routine-Entlassungsdaten ein Vergleich zwischen verschiedenen Spitälern bei vordefinierten Krankheitsbildern über festgelegte Indikatoren generiert. Auch der Schlaganfall in all seinen Facetten ist wegen seiner Häufigkeit und finanziellen Auswirkungen eines dieser Schlüsselkrankheitsbilder. Konkret werden zum Schlaganfall mehrere ICD-10-Diagnosen seit 2013 mit dieser Methodik monitiert (Tab. 1). Da ursprünglich maximal 60% all dieser Patienten an Stroke Units aufgenommen waren, wurde mit 2018 die Dokumentationspflicht auf alle Abteilungen, die solche Patienten behandeln, ausgedehnt. Nun gibt es durch Übermittlung eines „LKF basic dataset“ für alle Schlaganfälle, die in Österreich stationär behandelt werden, eine Datenbank aus Abrechnungsdaten im Bundesministerium. Mithilfe eines Ampelsystems und des Vergleichs mit deutschen Krankenhausdaten werden ganze Spitäler im Behandlungsprozess dargestellt. Die Leistungen einzelner Abteilungen sind dabei unerheblich. Bei relevanten Abweichungen vom statistischen Mittel muss das Spital eine Stellungnahme abgeben und kann auch in einem „Peer review“-Verfahren kommissionell überprüft werden.
2019 wurde von der AHA/ASA eine aktualisierte Empfehlung zum Schlaganfallbehandlungsprozess mit acht Paketen publiziert (Adeoye et al., Stroke 2019). Neben Primär- und Sekundärprävention von Schlaganfällen und ausreichender Schlaganfallrehabilitation steht hier eine wesentliche Frage im Zentrum:
Wie kommt ein Patient mit akutem Schlaganfall zeitgerecht ins richtige Behandlungszentrum?
Mit der zunehmenden Spezialisierung der Spitäler kann nicht mehr jedes Krankenhaus die volle Palette der Schlaganfallakuttherapie anbieten. Gleichzeitig kann nicht jeder Schlaganfallpatient direkt in ein „comprehensive stroke center“, in dem das komplette Behandlungsspektrum im 24/7-Modus verfügbar ist, gebracht werden. Ob also der jeweilige Patient nun eine Stroke Unit, eine endovaskuläre Thrombektomie oder eine Neurochirurgie benötigen wird, muss bis zu einem gewissen Ausmaß rasch PRÄHOSPITAL entschieden werden.
Das klinische Bild eines Schlaganfalles jedoch kann durch viele Ursachen bedingt sein – Ischämie, Blutung, Sinusvenenthrombose, postiktal, Migräne mit Aura und seltenere Ätiologien. Deshalb ist zwar die klinische Einschätzung des Schweregrades durch einen prähospitalen Score anhand der Symptome wertvoll, aber ohne akute zerebrale Bildgebung relativ unspezifisch. International wurden mehrere prähospitale Schlaganfall-Scores entwickelt (z.B. FAST, RACE), um den Rettungssanitätern die Früherkennung des Schlaganfalles zu erleichtern und den zeitkritischen Zutransport in eine passende Stroke Unit zu sichern. Diese Scores zeigen eine gewisse Sensitivität, aber geringe Spezifität für die Ätiologie des klinischen Syndroms und sind somit in Zeiten des wachsenden Therapiespektrums nicht ausreichend für die Festlegung des passenden Behandlungsortes eines Patienten.
Deshalb wurde vor mehr als 10 Jahren in Deutschland das neue Konzept einer „mobilen Stroke Unit (MSU)“ für Großstädte entwickelt. In einem umgebauten LKW kommen medizinisches Personal (Rettungssanitäter, Neurologe als Notarzt), Bildgebung und Labor direkt zum Patienten (siehe Abb. 2). Solche MSU gibt es mittlerweile international in mehr als 20 Städten weltweit. Die meiste Evidenz gibt es aus Berlin, wo nicht nur die maximale Treffsicherheit dieser modernen Form der prähospitalen Triage gezeigt wurde, sondern auch ein Behandlungsvorteil der MSU-zutransportierten Patienten im Vergleich mit der Standardtherapie (Helwig et al., JAMA Neurol 2019; Audebert et al., International Stroke Conference 2020).
Bei der virtuellen ESO-WSO-Tagung im November 2020 wurden auch vielversprechende Daten der MSU-Behandlung aus Melbourne/Australien gezeigt, wo eine Verkürzung der Behandlungszeiten sowohl für die systemische Thrombolyse als auch für die endovaskuläre Thrombektomie belegt werden konnte. Als Standard der akuten zerebralen Bildgebung wurde dort sowohl eine CCT als auch eine CTA der Hirnbasisgefäße direkt in der MSU durchgeführt.
Therapie des akuten zerebralen Großgefäßverschlusses
Seit 2016 ist die endovaskuläre mechanische Thrombektomie von akuten Verschlüssen der vorderen Zirkulation eine Standardbehandlung, weil bei richtiger Patientenselektion das Behandlungsergebnis erheblich besser ausfällt als bei der Kombination von systemischer Thrombolyse mit Stroke-Unit-Behandlung. Es handelt sich mit einer „number needed to treat“ von 2,6 um eine der effektivsten Therapien überhaupt (HERMES-Collaborators-Metaanalyse, 2016). Dennoch sind Zeitfenster, Reihenfolge der Behandlung (van Meenen et al., J Neurol 2020) und auch Fragen der verwendeten Devices bzw. Sedierung noch in laufender wissenschaftlicher Diskussion (Turc et al., Eur Stroke J 2019).
Auch die Organisationsformen der Zuweisung in das Interventionszentrum werden oft durch historische, geografische und regionale Gegebenheiten bestimmt. Es gibt das „Mothership“- und das „Drip-and-ship“-Konzept, aber keine „One size fits all“-Regel für alle Regionen. Auch die Frage, ob systemische Thrombolyse und endovaskuläre Thrombektomie bei akuten Verschlüssen großer Gehirngefäße immer kombiniert werden sollen, ist nicht restlos geklärt.
Eine rezente chinesische Studie zur Kombinationstherapie Thrombolyse plus Thrombektomie versus Thrombektomie alleine (Yang et al., NEJM 2020) zeigte nicht nur die Gleichwertigkeit der Behandlungsarme in dieser asiatischen Population, sondern auch die Hindernisse der Selektion für eine in China offenbar im Notfall kostenpflichtige Akutbehandlung.
Essenziell für eine gute Qualität dieser spitzenmedizinischen Leistung sind laut AHA Ausbildung, Standardisierung, Erarbeitung gemeinsamer Behandlungsprotokolle und Monitierung der Ergebnisqualität. Dies ist in Österreich bereits vielerorts Realität (Hofmarcher et al., factbook 2019).
In Katalonien wurde soeben eine große randomisierte klinische Studie zum Vergleich der beiden erwähnten Versorgungskonzepte beim akuten zerebralen Großgefäßverschluss fertiggestellt. Die dortige Versorgungslandschaft umfasst 28 Stroke Units und 6 Thrombektomie-Zentren und ist etwa vergleichbar mit Österreich. Bei insgesamt 1401 Patienten mit schwerem klinischem Schlaganfallsyndrom (RACECAT; Oral Presentation, virtual ESOC-WSO 2020) wurden für „drip-and-ship“ im Vergleich zu „mothership“ die gleiche Wirksamkeit und Sicherheit dokumentiert. Die Behandlungserfolge drei Monate nach dem Schlaganfall waren in beiden Gruppen gleich. Wenn also die Behandlungskette generell gut organisiert ist, soll man primäre Stroke Units ohne Thrombektomie-Angebot nicht aus dem Akutmanagement schwerer Schlaganfälle herausnehmen.
Ein anderes Konzept für die Durchführung der endovaskulären Thrombektomie ist das „Drip-and-drive“-Prinzip, das in Hamburg erprobt wird. Dort führen die primären Stroke Units die systemische Thrombolyse am Patienten durch, während gleichzeitig ein Interventionsteam per Bodentransport zum Schlaganfallpatienten fährt und der Eingriff lokal vorbereitet wird.
Sicherung des Behandlungserfolges – zerebrovaskuläre Sekundärprävention
Die nicht unerhebliche Rezidivgefahr, besonders in den ersten Wochen „post-stroke“, und auch das enorme Demenzrisiko nach Schlaganfall sind wesentliche Gründe für die Empfehlung der strikten Einstellung aller vaskulären Risikofaktoren nach einem Schlaganfall. Dennoch müssen Risikofaktoren nach einem Schlaganfall oft erst detektiert (z.B. paroxysmales Vorhofflimmern in ca. 30% aller Schlaganfallpatienten) und dann behandelt werden. Auch die permanente Abstinenz nach Entwöhnung bei Nikotinabusus (ebenso bei >30% aller Schlaganfallpatienten) stellt eine große Herausforderung in der „Post-stroke“-Phase dar. All dies muss parallel zur eventuell nötigen Schlaganfallrehabilitation aufgrund von funktionellen Defiziten organisiert werden.
Spitalsträger in Österreich versuchen zunehmend, stationäre Behandlungskosten der Rehabilitation in den LKF-externen Bereich auszulagern. Dem steht der oben ausgeführte duale Behandlungsbedarf der meist schwer kranken Schlaganfallpatienten gegenüber, die ohne die Rehabilitationsbetten in den Akutspitälern kaum fit für Rehabilitationszentren werden. Hier müssen Fachgesellschaften und medizinische Führungskräfte laufend in diversen Gremien Bewusstsein für die realen medizinischen Bedürfnisse von Schlaganfallpatienten schaffen. Auch die Etablierung einer neuen ambulanten Leistung im Sinne der „Schlaganfallnachsorge“ ist in den Verhandlungen ein wesentliches Ziel.
Covid-19-Pandemie
Die seit fast einem Jahr neue weltweite Herausforderung für den gesamten Schlaganfallversorgungsprozess hat alle Beteiligten vor neue Fragen gestellt. Ärzte sind mit einer Flut von Publikationen konfrontiert, bei denen die Möglichkeit der Verallgemeinerung der Beobachtungen oft zweifelhaft bleibt. Jedenfalls scheint in der „ersten Welle“ im Frühjahr 2020 die Anzahl der akuten Schlaganfallpatienten vielerorts reduziert gewesen zu sein, sei es, weil es weniger Ereignisse im Lockdown gab oder weil die Patienten das Spital nicht erreichten. Ebenso zeigte sich, dass gut organisierte und bewährte Gesundheitssysteme den vielfältigen Belastungen standhielten und die Versorgung der akuten Schlaganfallpatienten besser gewährleisten konnten als weniger stabile Versorgungssysteme. Dennoch bleibt durch die prolongierte Pandemie-Situation die Notwendigkeit der Sicherung der fachspezifischen Schlaganfallbehandlung nach State of the Art für die Patienten bei gleichzeitig gefordertem Mitarbeiterschutz und Ressourcenschonung stationärer Bettenkapazitäten eine enorme Herausforderung. Dies bedeutet für medizinische Teams eine laufende lokale Adaptation der Behandlungspfade als Zusatzaufgabe zum bekannten Versorgungsauftrag.
Fazit
Zusammenfassend war dies eine Momentaufnahme zur spannenden Frage: Wie organisiert man lokal/regional/national die Schlaganfallversorgung am besten, um mit ökonomischer Vernunft ein adäquates Behandlungsergebnis für den Patienten zu erreichen? Ebenso wichtig wie die wissenschaftliche Aufarbeitung offener Fragen und die kontinuierliche Qualitätssicherung bleibt aber eine nachhaltige und konstruktive Kooperation aller am Versorgungsprozess beteiligten Menschen.
Literatur:
bei der Verfasserin
Das könnte Sie auch interessieren:
Wie lässt sich die Zeit bis zur Diagnose der amyotrophen Lateralsklerose verkürzen?
Die amyotrophe Lateralsklerose (ALS) gilt als unaufhaltsam fortschreitende neurodegenerative Erkrankung, die im Durchscnitt drei bis vier Jahre nach Symptombeginn mit dem Tod durch ...
Ist die ketogene Diät eine Präzisionsmedizin?
Die ketogenen Ernährungstherapien sind etablierte Behandlungsformen bei Epilepsie. Während sie primär bei therapierefraktären pädiatrischen Epilepsien eingesetzt werden, finden sie ...
Neues aus der Alzheimer’s Disease Drug Development Pipeline
Mit der weltweiten Zulassung der Amyloidantikörper Lecanemab und Donanemab ist erstmals eine kausale Behandlung der Alzheimerkrankheit möglich geworden. Die Behandlung setzt an der ...